Samenvatting
Voor de behandeling van schizofrenie wordt gebruikgemaakt van anti-psychotica. Bij de keuze van het anti-spychoticum wordt, vanwege vergelijkbare effectiviteit, ook gekeken naar patiëntkenmerken. Lurasidon (Latuda®) is door registratie aan de keuzemogelijkheden toegevoegd. Uit de klinische onderzoeken is gebleken dat het effectiever is in het bestrijden van de psychose dan placebo. In vergelijkende onderzoeken met olanzapine en rispiridon werd geen verschil in werkzaamheid gezien. De meest voorkomende bijwerking is acathisie. Lurasidon geeft echter minder extrapiramidale bijwerkingen dan haloperidol. Ten opzichte van de andere anti-psychotica geeft het relatief weinig metabole problemen. Gezien de ruime keuze en de beperkte ervaring die er is met lurasidon, zal het niet direct een middel van eerste keuze worden.
M.A. Bijlstra-Cramer en R.W.G. Bruggeman, onder medeverantwoordelijkheid van de redactie
Pharma Selecta 2015 (februari) nr 1
Abstract
Antipsychotics are used for the treatment of schizophrenia. Given the similar efficacy of available antipsychotics, the drug choice is also based on patient characteristics. Lurasidone (Latuda®) has recently been approved for this indication. Clinical trials have shown that it is more effective than placebo in treating psychosis, and that it is as effective as olanzapine and risperidone. The most common side effect is akathisia. Lurasidone gives rise to fewer extrapyramidal side effects than haloperidol and causes relatively few metabolic problems compared with other antipsychotics. Given the broad choice of antipsychotics available and the limited experience with lurasidone, the new drug will not immediately become the drug of first choice.
Pharm Sel 2015;31:2-5.
Inleiding
Schizofrenie is een psychiatrische stoornis die wordt gekenmerkt door verschillende symptomen.1 Het kan gaan om positieve en negatieve kentekenen.2 Onder positieve wordt onder andere verstaan: wanen, hallucinaties, onsamenhangend spreken en katatonie (verstoring in de motoriek). Negatieve verschijnselen zijn onder meer: emotionele terugtrekking, depressie, passiviteit, weinig en niet vloeiend kunnen spreken.
De diagnose schizofrenie kan worden gesteld bij twee of meer symptomen die langer dan een maand aanwezig zijn.1 In het geval van bizarre wanen of hallucinaties in de vorm van commentaar op gedachten of meerdere stemmen is slechts één symptoom nodig. Het algemeen functioneren moet verminderd zijn; dit kan tot uiting komen in persoonlijke verzorging of op het werk. Daarnaast zijn er nog verschillende andere aspecten die meegenomen worden voor het stellen van de diagnose.
De incidentie is ongeveer 1,5 op tienduizend per jaar. De schatting is dat in Nederland ongeveer 120 duizend mensen lijden aan schizofrenie.
Voor de behandeling van schizofrenie kan geput worden uit de groep anti-psychotica. Hierbij wordt de keuze niet alleen gemaakt op basis van effectiviteit van het middel, maar worden ook patiëntkenmerken en -voorkeuren meegenomen. De effectiviteit van de verschillende anti-psychotica is namelijk vergelijkbaar. Het enige anti-psychoticum dat er in onderzoek beter uitkwam, was clozapine. Clozapine is echter geen eerste keuze vanwege het risico op agranulocytose en de controles die daarom noodzakelijk zijn.
Dit artikel bespreekt het nieuwe anti-psychoticum lurasidon (Latuda®) dat is geregistreerd voor de behandeling van schizofrenie bij volwassenen van achttien jaar en ouder.
Farmacologie
Dynamiek
Lurasidon bindt aan verschillende receptoren, waardoor het effect tot stand komt.3 Het gaat om D2-receptoren en het serotonerge 5-HT2A en 5-HT7. Daarnaast bindt het aan alfa 2a- en alfa 2c-receptoren. Op deze receptoren heeft het een antagonerend effect. Verder is het een partiële agonist van de 5-HT1A-receptor. Lurasidon bindt niet aan cholinergereceptoren. Het wordt ook nog in twee actieve metabolieten omgezet.
Kinetiek
De Cmax wordt bereikt na ongeveer één tot drie uur. Gemiddeld stijgt de Cmax twee- tot driemaal wanneer het ingenomen wordt met voedsel.3 Voor een groot deel wordt lurasidon gebonden aan eiwitten in het bloed. Metabolisme van lurasidon vindt voornamelijk plaats via CYP3A4. In de afbraak wordt lurasidon omgezet in onder andere twee actieve en twee niet-actieve metabolieten. Lurasidon is een substraat en een remmer van P-gp en BCRP. De halfwaardetijd is 20-40 uur. Ongeveer 67% wordt via de feces uitgescheiden en 19% via de urine. Binnen de aanbevolen dosering van 20-160 mg is er sprake van een lineaire kinetiek. Steady state wordt bereikt binnen zeven dagen na starten van lurasidon.
Klinisch onderzoek
Er zijn verschillende, gepubliceerde fase 2/3-onderzoeken uitgevoerd met lurasidon. Bij al deze onderzoeken zijn patiënten geïncludeerd die bekend waren met schizofrenie, waarbij een acute verslechtering optrad die opname noodzakelijk maakte.4-7 Deze fase 3-onderzoeken besloegen allemaal zes weken. Daarnaast is er een onderzoek uitgevoerd waarbij patiënten gedurende een jaar gevolgd werden om de effectiviteit en veiligheid vast te stellen – dit werd vergeleken met rispiridon.8 De studie naar langetermijneffecten is uitgevoerd op klinisch stabiele patiënten. Ook is lurasidon al meegenomen in een grote meta-analyse, waarin vijftien anti-psychotica vergeleken worden.9
Van de fase 3-onderzoeken waren er drie met verschillende doseringen lurasidon versus placebo. In één onderzoek werd ook nog een vergelijking met olanzapine gemaakt. In de meeste onderzoeken werd gebruik gemaakt van de Brief Psychiatric Rating Scale (BPRSd), deze is afgeleid van de Positive and Negative Syndrome Scale (PANSS). In deze onderzoeken kunnen subscores bepaald worden op positieve symptomen, negatieve symptomen en algemene psychopathologie. Daarnaast is in de meeste onderzoeken gebruikgemaakt van de Clinical Global Impression of Severity (CGI-S), deze geeft een maat voor de ernst van de aandoening. In de studie waar gekeken is naar de effectiviteit en verdraagbaarheid gedurende één jaar, was de intentie een test te doen op inferioriteit. Deze bleek echter niet uitvoerbaar omdat er veel minder patiënten een terugval kregen dan verwacht. Ten opzichte van risperidon waren de PANSS en de CGI-S niet significant verschillend na een jaar.8 In alle vergelijkingen met placebo was lurasidon significant effectiever.4-8 Bij de studie waarbij lurasidon vergeleken werd met olanzapine was geen significant verschil in effectiviteit op de PANSS en de CGI-S.5 Bij één studie kon geen effect worden gezien bij 40 en 120 mg maar wel voor de dosering van 80 mg per dag. Een mogelijke verklaring van dit resultaat was dat er een relatief hoge placeborespons werd gezien.7
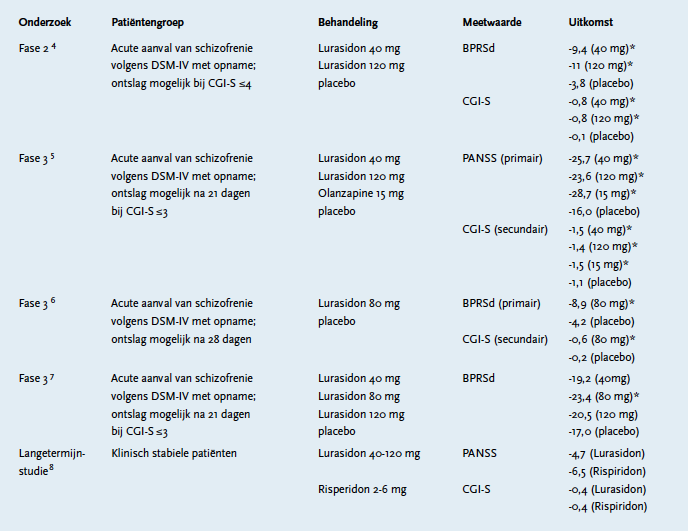
Tabel 1 Samenvatting van de verschillende effectiviteitsstudies
*statistisch significant ten opzichte van placebo 9
Bijwerkingen
De meest voorkomende bijwerkingen van lurasidon zijn acathisie (bewegingsdrang) en somnolentie; deze bijwerking treedt op bij meer dan één op de tien gebruikers. Daarbij is tot 111 mg een dosisafhankelijke relatie waargenomen.3
In vergelijking met olanzapine werd meer acathisie gezien op lurasidon: bij de groep die 120 mg gebruikte kwam dit bij 22,9% voor, bij de 40 mg-groep nog bij 11,8%, tegenover 7,4% van de olanzapinegebruikers.5 Met betrekking tot gewichtstoename viel de vergelijking uit in het nadeel van de olanzapine: 34,4% van de olanzapinegebruikers kwam meer dan 7% aan; terwijl dit voor beide groepen lurasidon gecombineerd slechts voor 5,9% van de gebruikers het geval was.
In de langetermijnstudie, waarbij gedurende een jaar risperidon of lurasidon gebruikt werd, waren de drie meest voorkomende bijwerkingen voor lurasidon: misselijkheid, slapeloosheid, en sedatie.8 Voor risperidon was de top drie van de meest voorkomende bijwerkingen: gewichtstoename, slaperigheid en hoofdpijn. Het aantal patiënten dat extrapiramidale verschijnselen ondervond was voor beide groepen vergelijkbaar.
In de meta-analyse van vijftien anti-psychotica is ook het optreden van bijwerkingen vergeleken.9 Hierin is te zien dat lurasidon op twee na de minste gewichtstoename veroorzaakt, na haloperidol en ziprasidon (wat niet in Nederland te verkrijgen is). Volgens de SPC wordt gewichtstoename gezien bij 1-10 op 100 gebruikers, waarmee het een veel voorkomende bijwerking is.
Het meest wordt gestopt met haloperidol vanwege het optreden van extrapiramidale bijwerkingen. In vergelijking met haloperidol geeft lurasidon minder extrapiramidale bijwerkingen – hoewel acathisie de meest voorkomende bijwerking van lurasidon is.
Interacties
Voorzichtigheid is geboden bij het voorschrijven van lurasidon in combinatie met middelen die het QT-interval kunnen verlengen.3 Het is niet duidelijk op grond waarvan dit geadviseerd wordt en wat dit inhoudt. In geen van de klinische studies werd een verlenging van het QT-interval gezien ten opzichte van placebo. Lurasidon wordt niet vermeld op de website www.crediblemeds.org waar middelen die QT-verlenging geven, geclassificeerd worden.10 Mogelijk is er nog niet voldoende over bekend, alhoewel lurasidon sinds 2010 door de FDA is goedgekeurd voor de Amerikaanse markt.11
Lurasidon en een actieve metaboliet worden afgebroken door CYP3A4.3 Combinaties van lurasidon met CYP3A4-remmers kunnen daarom zorgen voor een verhoogde blootstelling aan lurasidon. Sterke remmers zoals ketoconazol zorgen voor een zes (actieve metaboliet) tot negen (lurasidon) keer hogere blootstelling, waar matige remmers voor een twee- tot vijfmaal hogere blootstelling zorgen.
Hoewel dit niet specifiek is onderzocht, wordt de combinatie met grapefruitsap ontraden, omdat dit ook een CYP3A4-remmer is.
In combinatie met sterke CYP3A4-inductoren is de blootstelling aan lurasidon verminderd.12 In combinatie met rifampicine kan dit tot zes keer verminderd zijn. Bij matige en zwakke inductoren kan dit waarschijnlijk tot tweemaal verminderd zijn – daar moet tot twee weken na het staken van de inductor rekening mee gehouden worden.
Contra-indicaties
Overgevoeligheid voor lurasidon of een van de hulpstoffen is een contra-indicatie.3 Verder wordt de combinatie met sterke CYP3A4-remmers genoemd als contra-indicatie.
Bij een lichte nierfuntiestoornis is het niet nodig om de dosering aan te passen. Bij een nierfunctiestoornis, waarbij de creatinineklaring <50 ml/min is, wordt aanbevolen met een halve hoeveelheid te starten en niet hoger van 74 mg te doseren.
Bij een leverfunctiestoornis Child Puch klasse B (matig) en C (ernstig) is het nodig om de dosering aan te passen. Startdosering is 18,5 mg met als maximum 74 mg bij een matige stoornis en 37 mg bij een ernstige leverfunctiestoornis. Bij een lichte leverfunctiestoornis is het niet nodig de dosering aan te passen.
Zwangerschap en lactatie
Er is weinig bekend over het gebruik van lurasidon tijdens zwangerschap.3 Ook dieronderzoeken hebben weinig informatie opgeleverd. Mogelijke risico’s van het gebruik tijdens zwangerschap kunnen dus niet aangegeven worden. Gebruik tijdens de zwangerschap wordt daarom ontraden.
Bij ratten wordt lurasidon in de moedermelk uitgescheiden. Daarom moet een afweging gemaakt worden tussen de noodzaak voor de moeder en het mogelijke risico voor de baby.
Handelspreparaat, dosering en prijs
Lurasidon wordt op de markt gebracht onder de naam Latuda® door Takeda Pharma, in tabletten van 18,5, 37 en 74 mg. De tabletten van 37 mg komen overeen met 40 mg lurasidonhydrochloride dat gebruikt is in de onderzoeken en de tabletten van 74 mg met 80 mg uit de onderzoeken.3 Startdosering is 37 mg, waarbij ophoging van de dosering nodig is bij onvoldoende klinische respons, welke door de arts te beoordelen is. De maximaal aanbevolen dosering is 148 mg. Wanneer de behandeling bij een dosering boven de 111 mg langer dan drie dagen onderbroken is, wordt geadviseerd om eerst bij 111 mg te beginnen en vandaar weer op te bouwen. Het is belangrijk om het middel met voedsel in te nemen vanwege de betere opname. De tabletten zijn film-omhuld om de bittere smaak te maskeren. De sterktes 37 mg (AIP 68,32 euro; 28 stuks) en 74 mg (AIP 136,85 euro; 28 stuks) zijn verkrijgbaar in Nederland.13
Conclusie en plaatsbepaling
Lurasidon is in onderzoek ten opzichte van placebo effectiever gebleken in de behandeling van een acute verslechtering bij patiënten met schizofrenie. In de huidige richtlijn wordt aangegeven dat het niet mogelijk is een voorkeursmiddel aan te wijzen op basis van effectiviteit of werkzaamheid. De keuze wordt gebaseerd op bijwerkingenprofiel, specifieke patiëntkenmerken en welbevinden. Aan de keuzemogelijkheden kan lurasidon toegevoegd worden. Mogelijke voordelen zijn dat het relatief weinig gewichtstoename geeft en – ten opzichte van haloperidol – minder extrapiramidale bijwerkingen, waardoor het een alternatief kan zijn als haloperidol niet verdragen wordt.
Gezien de ruime keuze en de beperkte ervaring met lurasidon, zal het niet direct het middel van eerste keuze worden. Ook de effectiviteit is vergelijkbaar met die van andere middelen. Het blijft een kwestie van afwegen wat acceptabel wordt gevonden op basis van bijwerkingen.
Literatuur
1 http://www.ggzrichtlijnen.nl/uploaded/docs/Multidisciplinaire%20richtlijn%20Schizofrenie%202012.pdf (geraadpleegd 26-08-2014).
2 Stahl’s essential psychopharmacology; third edition. Stahl 2008.
3 SPC Lurasidon via http://www.ema.europa.eu/docs/nl_NL/document_library/EPAR_-_Product_Information/human/002713/WC500164683.pdf.
4 Ogasa M, Kimura T, Nakamura M, Guarino J. Lurasidone in the treatment of schizophrenia: a 6-week, placebo-controlled study. Psychopharmacology 2013;225:519-530.
5 Meltzer HY, Cucchiaro J, Silva R et al. Lurasidone in the treatment of schizophrenia: a randomized, double-blind, placebo- and olanzapine-controlled study. Am J Psychiat 2011;168:957-967.
6 Nakamura M, Ogasa M et al. Lurasidone in the treatment of acute schizophrenia: A double-blind, placebo-controlled trial. J Clin Psychiat 70:6, June 2009.
7 Nasrallah HA, Silva R et al. Lurasidone for the treatment of acutely psychotic patients with schizophrenia: A 6-week, randomized, placebo-controlled study. J Psychiat Res 47 (2013) 670e677.
8 Citrome L, Cucchiaro J et al. Long-term safety and tolerability of lurasidone in schizophrenia: a 12-month, double-blind, active-controlled study. Int Clin Psychopharm 2012;27:165-176.
9 Leucht S, Cipriani A et al. Comparative efficacy and tolerability of 15 antipsychotic drugs in schizophrenia: a multiple-treatments meta-analysis. Lancet 2013;382:951-962.
10 Geneesmiddeldatabase over QT-verlenging via: www.crediblemeds.org (geraadpleegd 22-1-2015).
11 Voorschrijfinformatie van de FDA via: http://www.accessdata.fda.gov/drugsatfda_docs/label/2013/200603lbls10s11.pdf (geraadpleegd 5-2-2015).
12 SPC via: http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Product_Information/human/002713/WC500164683.pdf (geraadpleegd 5-2-2014).
13 Handelsproductinformatie op KNMP kennisbank (geraadpleegd januari 2015).