Samenvatting
Snelwerkend insuline aspart (Fiasp®) is een formulering van insuline aspart met niacinamide (vitamine B3) en L-arginine als adjuvantia. Door deze toevoegingen werkt deze insuline aspart negen minuten sneller. In kleine, korte studies lijkt een gelijkwaardigheid tussen snelwerkend en gewoon insuline aspart op reductie van HbA1c- en postprandiale glucosespiegels. In slechts één langer durende studie van 52 weken werd een positief verschil gevonden ten gunste van snelwerkend insuline aspart. In de overige grote studies tot 26 weken kon de meerwaarde niet worden aangetoond. Interessant is wel dat in een van deze studies een gelijkwaardig effect werd gezien 0 tot 2 minuten vóór de maaltijd of toediening ná de maaltijd. Hierdoor heeft de diabetespatiënt een grotere flexibiliteit in het tijdstip van injecteren. Aanvullende studies moeten uitwijzen of snelwerkend insuline aspart ook écht iets extra’s kan betekenen voor de type 1 of 2 diabeet. Op dit moment is dat (nog) niet het geval.
E.C. Weening en A. Heersche, onder medeverantwoordelijkheid van de redactie
Abstract
Fast-acting insulin aspart (Fiasp®) contains niacinamide (vitamin B3) and L-arginine as adjuvants. This combination works 9 minutes faster than insulin aspart alone. Small, short studies have shown fast-acting and normal insulin to cause a similar reduction in HbA1c and postprandial glucose levels. Only one longer study over 52 weeks found a positive effect of fast-acting insulin aspart, whereas large studies with a 26-week follow-up did not find fast-acting insulin aspart to provide extra benefit. However, one of these studies showed that fast-acting insulin aspart had a similar action whether administered 0-2 minutes before a meal or after a meal. This provides a greater flexibility in the timing of administration. Further studies are needed to demonstrate whether fast-acting insulin aspart has added benefit in patients with type 1 or 2 diabetes.
Pharma Selecta 2018 (mei) Pharm Sel 2018;34:38-41
Inleiding
Insuline is een eiwit dat wordt geproduceerd en uitgescheiden door de bètacellen van de eilandjes van Langerhans in de alvleesklier, in respons op een verhoging van de plasmaglucosespiegel. Het zorgt voor omzetting van glucose in glycogeen in lever en spierweefsel, versterkt aldaar de eiwitsynthese, verbetert de glucose- en aminozuuropname in spierweefsel en versterkt de opslag en synthese van triglyceriden in vetweefsel. Insuline bestaat uit twee eiwitketens, de alfa- en bètaketen, met elkaar verbonden door twee zwavelbruggen. In de bètacel aggregeert insuline met zink tot hexameren en, na afgifte in de bloedbaan, dissocieert dit tot dimeren en uiteindelijk tot de actieve monomere vorm.[1]
Bij type 1 en 2 diabeten heeft de behandelaar de beschikking over een breed assortiment kort-, middellang- en langwerkende insuline. Omdat er de laatste jaren veel nieuwe varianten geïntroduceerd zijn, volgt hier een opsomming:
Kortwerkende insuline-analoga – Dit zijn monomeren die zich kenmerken door één of twee aminozuursubstituties op de bètaketen. Insuline aspart (Fiasp®, Novorapid®, B28-substitutie asparaginezuur in plaats van proline), insuline glulisine (Apidra®, B29- en B3-substitutie van respectievelijk glutaminezuur in plaats van lysine, en lysine in plaats van asparaginezuur) en insuline lispro (Humalog®, verwisseling van lysine en proline op B28 en B29).[1 2]
Langwerkende insuline-analoga – Deze kenmerken zich door weer een andersoortige aanpassing aan de eitwitketens. Bij insuline detemir (Levemir®) is threonine op B30 verdwenen en is een vetzuurketen gekoppeld aan B29. Dit verhoogt de complexvorming van insuline en versterkt de binding met albumine, waardoor een depoteffect ontstaat in de huid. Bij insuline glargine (Lantus®) zijn aminozuursubstituties toegepast op A21, glycine in plaats van asparaginezuur, en aan de B-keten twee extra asparaginezuur. Hierdoor is de insuline minder oplosbaar bij fysiologische pH en ontstaat na injectie een neerslag met depoteffect in de huid. De laatste loot aan deze tak is insuline degludec (Tresiba®). Deze kenmerkt zich door vervanging van threonine op B30 door een vetzuurketen. Dit resulteert in de vorming van oplosbare multihexameren met depoteffect in de huid.[1 2]
Mix-varianten – De lispro- en aspartvariant zijn ook beschikbaar als complex met protamine voor een middellange werking en als zodanig verwerkt in combinatie met de kortwerkende variant (Humalog Mix® en Novomix®). De aspart is eveneens met insuline degludec als mix verkrijgbaar (Ryzodeg®).[1 2]
Ondanks het feit dat met de komst van de snel- en kortwerkende insuline-analoga de glucosecontrole van type 1 en type 2 diabeten enorm verbeterd is, kennen deze middelen nog steeds beperkingen. Zo is de afgifte van een kortwerkend insuline (aspart, glulisine, lispro) na injectie aan de bloedbaan significant trager dan de fysiologische, postprandiale insulineafgifte aan de hepatische circulatie. Bij jonge kinderen kan er een extra vertraging optreden, omdat ouders er vaak voor kiezen nà de maaltijd de insuline te spuiten, waarbij het aantal eenheden vaak afhangt van de omvang van de maaltijd.[3]
De firma Novo-Nordisk brengt nu een formulering van de insuline aspart op de markt, waarmee een snellere insulinevrijgifte in het bloed te realiseren is: snelwerkend insuline aspart (Fiasp®) ook wel faster-acting insulin-aspart. Hiermee zou een betere benadering van de endogene prandiale insulinespiegel mogelijk moeten worden.[4]
Verbetering van de glykemische controle is essentieel voor het verder kunnen terugdringen van microvasculaire complicaties bij type 2 diabeten.[4]
Farmacologie
Dynamiek
Snelwerkend insuline aspart is een formulering van insuline aspart (IAsp) met niacinamide (vitamine B3) en L-arginine als adjuvantia. Niacinamide zou een snellere initiële absorptie vanuit de subcutane injectieplaats geven. L-arginine is als stabilisator voor niacinamide toegevoegd. In experimentele in vitro studies is de doordringingssnelheid van IAsp in aanwezigheid van niacinamide gemeten. Hieruit bleek dat niacinamide de monomere fractie van IAsp in de subcutis met 35% en de transendotheliale doordringing van IAsp met 27% verhoogt. De verhoging van de monomere fractie verklaart de snellere absorptiesnelheid.[3 4]
Kinetiek
De biologische beschikbaarheid van snelwerkend IAsp na subcutane toediening is circa 80%. De tijd tot 50% van de Cmax is circa negen minuten korter bij snelwerkend IAsp in vergelijking met IAsp. Tmax voor IAsp is na subcutane toediening 40-60 minuten. Snelwerkend IAsp heeft een lage bindingsaffiniteit voor plasma-eiwitten (<10%), vergelijkbaar met reguliere humane insuline. Het verdelingsvolume van 0,22 l/kg komt overeen met het extracellulaire vochtvolume in het lichaam.
De afbraak van snelwerkend IAsp gebeurt hoofdzakelijk in de lever en is vergelijkbaar met humane insuline. Geen van de gevormde metabolieten is actief. De halfwaardetijd van snelwerkend IAsp na subcutane toediening is 57 minuten en is vergelijkbaar met die van IAsp.[2 5]
Klinische studies
Er zijn met snelwerkend IAsp een drietal belangrijke klinische studies uitgevoerd bij zowel type 1 als type 2 diabeten.[5 6]
Onset 1-trial
Het Onset 1-onderzoek betreft een multicenter, gerandomiseerde, parallel opgezette, fase 3 ‘non-inferiority’ studie, waarbij de effectiviteit en veiligheid van snelwerkend IAsp vergeleken is met conventioneel IAsp bij volwassenen met diabetes type 1. Primair eindpunt: verandering van HbA1c ten opzichte van baseline na 26 weken. Na een run-in periode van acht weken werden vrijwilligers gerandomiseerd verdeeld over drie groepen: twee dubbelblind opgezette groepen, waarbij maaltijdgebonden injectie (0 tot 2 minuten voor de maaltijd) met snelwerkend IAsp (n=381) of IAsp (n=380) en een open-label groep met snelwerkend IAsp na de maaltijd (n=382) met elkaar werden vergeleken.
De HbA1c in week 26 daalde bij de snelwerkend-IAsp-maaltijdgroep van 59,3 naar 56,4 mmol/mol, bij de IAsp-maaltijdgroep van 59,7 naar 57,6 mmol/mol en bij de postmaaltijd-snelwerkend-IAsp-groep van 59,9 naar 58,6 mmol/mol. Hoewel de reductie in HbA1c voor snelwerkend-IAsp-maaltijd-groep statistisch significant groter was dan voor gewoon IAsp, kan niét geconcludeerd worden dat snelwerkend IAsp superieur is aan IAsp. De studieopzet staat dit niet toe. Qua veiligheid bleek snelwerkend IAsp bij de maaltijd in het eerste uur na de maaltijd meer kans te geven op hypoglykemie dan IAsp of snelwerkend IAsp postmaaltijd: 33,9%, 28,4% respectievelijk 22,5%. Als alle gevallen van hypoglykemie bij elkaar werd genomen, werd geen significant verschil gezien tussen de verschillende groepen.[7]
Vervolg Onset 1-trial
De Onset 1-studie besloeg een periode van 26 weken. In nog eens 26 weken daarna werd de veiligheid en effectiviteit van snelwerkend IAsp versus IAsp onderzocht. Na 52 weken bleek de verandering in HbA1c ten opzichte van baseline voor de maaltijdgebonden snelwerkend IAsp respectievelijk IAsp -1,2 en +0,03 mmol/mol. Het verschil tussen snelwerkend IAsp en IAsp bedroeg -1,04 mmol/mol (95% CI -2,05; -0,04). Een klein verschil, maar net wel statistisch significant. Ook de verandering ten opzichte van baseline in postprandiale glucose (PPG) één uur na de maaltijd bleek statistisch significant verschillend. Snelwerkend IAsp -1,05 mmol/L versus -0,14 mmol/L voor IAsp. De PPG twee, vier en zes uur na de maaltijd verschilde niet. Het vóórkomen van ernstige hypoglykemie overdag, één uur of twee uur na de maaltijd of ’s nachts bleek niet te verschillen tussen beide groepen.[8]
Onset 2-trial
Het Onset 2-onderzoek betreft een multicenter, dubbelblind, treat-to-target, ‘non-inferiority’ fase 3-studie, waarin de effectiviteit en veiligheid van snelwerkend IAsp versus IAsp bij volwassenen met diabetes type 2 vergeleken werd. Primaire eindpunt: verandering van HbA1c ten opzichte van baseline na 26 weken behandelen. Na een run-in periode van acht weken op basaal insuline werden de vrijwilligers gerandomiseerd verdeeld over twee groepen: maaltijdgebonden snelwerkend IAsp (n=345) of IAsp (n=344). In beide groepen werd gebruik gecombineerd met insuline glargine en metformine. Verandering in HbA1c ten opzichte van baseline was -15,1 mmol/mol voor snelwerkend IAsp en -14,9 mmol/mol voor IAsp. Zowel op baseline als na 26 weken waren de verschillen in HbA1c voor beide groepen niet significant. Hypoglycemie binnen twee uur na de maaltijd werden in de snelwerkend IAsp-groep significant vaker gezien dan bij de IAsp-groep (RR 1,60 [95% CI 1,13-2,27; p=0,0082]). Binnen één, vier en zes uur na de maaltijd werden geen significante verschillen in hypoglykemie waargenomen. Voor nachtelijk optredende hypo’s is er een trend waarneembaar ten nadele van snelwerkend IAsp (RR 1,38 [95% CI 0,96-2,00]).[9]
Onset 3-trial
De derde Onset-studie onderzocht de verbeterde glycemische controle van maaltijdgebonden snelwerkend IAsp aan een regime met basaal insuline en metformine. Primair eindpunt was verandering van de HbA1c vanaf baseline na 18 weken behandeling. Secundaire eindpunten waren: PPG-verandering en overall PPG, gewicht, ernstige bijwerkingen en hypoglykemie. In deze open-label, gerandomiseerde, 18 weken durende studie werden 236 volwassenen geïncludeerd met onvoldoende gereguleerde diabetes type 2 (HbA1c SD: 63,1 +/- 7,5 mmol/mol) die waren ingesteld op basaal insuline eenmaal daags en orale antidiabetica. Na een run-in van acht weken werden de patiënten 1:1 gerandomiseerd tot basaal-bolus insuline met snelwerkend IAsp en tot basaal-bolus insuline alleen. Beide groepen kregen additioneel metformine. Na 18 weken bleek de HbA1c gedaald van 63,2 naar 50,7 mmol/mol bij de combinatie met snelwerkend IAsp en van 63,2 naar 60,7 mmol/mol voor basaal insuline alleen. Een verschil voor snelwerkend IAsp van -10,3 mmol (-12,8; -7,8; p<0,0001). Een vergelijkbare daling werd gezien voor de gemiddelde, door de patiënt gemeten, glucosespiegel. Qua bijwerkingen werd vaker ernstige hypoglykemie gezien in de groep met snelwerkend IAsp: bij 58,3% versus 25,0% van de patiënten; daarnaast kwam enige gewichtstoename voor.[10]
Verder zijn er diverse kleine studies gedaan naar de verschillende effecten en eigenschappen van snelwerkend IAsp. Zo blijkt snelwerkend IAsp na injectie in het abdomen een snellere beschikbaarheid te hebben dan na injectie in het bovenbeen, resulterend in een Cmax-ratio=0,70 (injectie in bovenbeen/injectie in abdomen). Vergelijkbare ratio’s zijn bekend voor de andere kortwerkende insulinen.[11]
Ook is het gebruik van snelwerkend IAsp in een insulinepomp uitgebreid onderzocht. In de studie van Bode et al. (2017)[12] en Heise et al. (2016)[13] bleek snelwerkend IAsp een betere postprandiale glucosecontrole te geven dan IAsp.
Zijlstra et al. (2018)[14] onderzochten de verenigbaarheid en veiligheid van snelwerkend IAsp versus IAsp bij continue infusie. Er werd geen verschil gevonden in het aantal microscopisch bewezen occlusies van de infusieset tussen snelwerkend IAsp en IAsp.
In een poging om het onderliggend mechanisme van een lagere postprandiale glucosespiegel ten gevolge van snelwerkend IAsp nog beter te begrijpen, hebben Basu et al. (2018) een studie uitgevoerd bij 41 diabeten type 1. In een gerandomiseerd, dubbelblind, cross-over opgezette studie zijn vergelijkbare doseringen van snelwerkend IAsp en IAsp samen met een gestandaardiseerde glucose-houdende maaltijd met elkaar vergeleken op farmacokinetische eindpunten. De insulinespiegel in het eerste uur na de maaltijd was 32% hoger voor snelwerkend IAsp ten opzichte van IAsp. De vermindering van de postprandiale glucosespiegel bij snelwerkend IAsp bleek voor een deel verklaard door een grotere onderdrukking van de endogene glucoseproductie met 12% bij snelwerkend IAsp ten opzichte van IAsp. Vrije vetzuurspiegels bleken in het eerste uur na de injectie 36% lager te liggen voor snelwerkend IAsp dan voor IAsp.[15]
Bijwerkingen
De bijwerkingen zijn voor snelwerkend IAsp vergelijkbaar met IAsp. De meest voorkomende bijwerkingen betreffen hypoglykemie (zeer vaak >1/10), allergische huidreacties al of niet op de injectieplaats (vaak >1/100) en lipodystrofie (soms >1/1000).[5]
Interacties
Interacties zijn voor snelwerkend IAsp vergelijkbaar met IAsp. De volgende stoffen kunnen de insulinebehoefte verlagen: MAO-remmers, bètablokkers, ACE-remmers, salicylaten en anabole steroïden. Stoffen die de insulinebehoefte verhogen zijn: orale anticonceptiva, thiaziden, glucocorticoïden, schildklierhormonen, groeihormoon en danazol. Alcohol kan het hypoglykemisch effect van insuline versterken of verminderen.[5]
Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de hulpstoffen geldt als contra-indicatie.[5]
Zwangerschap en lactatie
Snelwerkend IAsp kan veilig gebruikt worden tijdens de zwangerschap en borstvoeding.[5]
Handelspreparaat, dosering en prijs
Snelwerkend insuine aspart (Fiasp®) is door Novo Nordisk in de handel gebracht met een sterkte van 100 IE/ml in injectieflacons van 10 ml, flextouch voorgevulde wegwerppennen van 3 ml en penfill-patronen van 3 ml. Fiasp® is geregistreerd voor de behandeling van diabetes mellitus bij volwassenen – dit in tegenstelling tot Novorapid® dat ook voor kinderen vanaf één jaar geregistreerd is. Fiasp® moet 0 tot 2 minuten voor het begin van de maaltijd subcutaan worden toegediend, met de mogelijkheid van toediening tot maximaal 20 minuten na het begin van de maaltijd.[5]
Eén eenheid Fiasp® komt overeen met één internationale eenheid humane insuline of één eenheid van andere snelwerkende insuline-analogen.[5]
Naast de eerder vermelde niacinamide en L-arginine, bevat Fiasp® de volgende andere hulpstoffen: fenol, metacresol, glycerol, zinkacetaat en dinatriumfosfaatdihydraat.
Fiasp® wordt volledig vergoed (www.medicijnkosten.nl, geraadpleegd 27-04-2018).
Discussie en conclusie
De firma Novo Nordisk heeft met snelwerkend insuline aspart (Fiasp®) een nieuw kortwerkend insuline in haar gamma. Uit de studies die ten grondslag liggen aan de registratie, blijkt een gelijkwaardigheid van snelwerkend insuline aspart met insuline aspart (IAsp). De studies zijn echter te klein en te kort (<26 weken) om tot enig serieus significant verschil te komen op de eindpunten HbA1c-verandering en reductie van de postprandiale glucosespiegel. Interessant is wel dat in een van deze studies een gelijkwaardig effect gezien werd voor snelwerkend IAsp bij toediening 0 tot 2 minuten vóór de maaltijd, als bij toediening ná de maaltijd. Hierdoor heeft de diabetespatiënt grotere flexibiliteit in het tijdstip van injecteren. In één onderzoek, de verlenging van de Onset 1-studie tot 52 weken, werd wél een verschil gezien tussen snelwerkend IAsp en IAsp op HbA1c en postprandiale glucosespiegel binnen één uur na de maaltijd, ten gunste van het snelwerkend IAsp.
Of snelwerkend IAsp, naast de snellere werking, ook écht een betere regulatie geeft van de HbA1c ten opzichte van de andere kortwerkende insulinen, zal in verder onderzoek vastgesteld moeten worden. Ook is een mogelijk verhoogde kans op het optreden van hypoglykemie op snelwerkend IAsp onduidelijk. In de verschillende studies zijn de waarnemingen wisselend. De algemene trend lijkt wel dat het risico op hypoglykemie met snelwerkend IAsp, hoewel niet significant, verhoogd is ten opzichte van IAsp. Verder onderzoek zal dit beeld moeten bevestigen of ontkrachten. De waarneming dat snelwerkend IAsp significante betere onderdrukking geeft van de endogene glucoseproductie en lagere postprandiale vetzuurspiegels, zal bevestigd moeten worden in de algemene populatie en in langer durende studies.
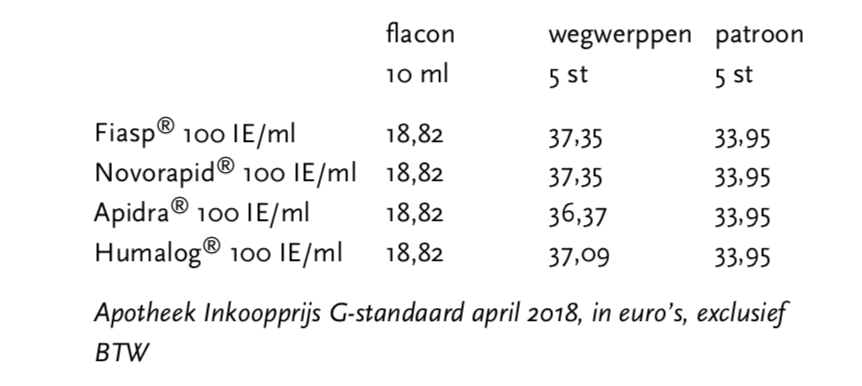
Qua prijs is Fiasp® gelijk aan Novorapid®, afkomstig van dezelfde firma, en is het vergelijkbaar met Apidra® van Sanofi en Humalog® van Lilly. Hiermee is snelwerkend insuline aspart een gelijkwaardig alternatief voor de andere soorten snelwerkende insuline.
Bij de moeilijk in te stellen diabeet, die kampt met chronisch te hoge HbA1c-spiegels en te hoge postprandiale glucosespiegels, ondanks goed gebruik van een kortwerkend insuline, zou snelwerkend IAsp ingezet kunnen worden. Kinderen onder de achttien die in deze categorie vallen, zullen moeten wachten tot het middel ook voor deze groep geregistreerd is.
Literatuur
1. Waller DG, Sampson AP. Medical Pharmacology & Therapeutisch, fourth edition 2014:457-461.
2. Farmacotherapeutisch Kompas. https://www.farmacotherapeutischkompas.nl/bladeren/groepsteksten/insulinen (geraadpleegd 16 april 2018).
3. Biester T, Kordonouri O, Danne T. Pharmacological Properties of Faster-Acting Insulin Aspart. Curr Diab Rep 2017;17:101.
4. Heise T, Pieber TR et al. Pharmacokinetic and Pharmacodynamic Properties of Faster-Acting Insulin Aspart versus Insulin Aspart Across a Clinically Relevant Dose Range in Subjects with Type 1 Diabetes Mellitus. Clin Pharmacokinet 2017;56:649-660.
5. SMPC Fiasp®, 03-02-2017, 11/11/2016 Fiasp -EMEA/H/C/004046 http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Product_Information/human/004046/WC500220890.pdf
6. EPAR symmary for the public Fiasp®, EMA/748368/2016 http://www.ema.europa.eu/docs/
7. Russell-Jones D, Bode BW et al. Fast-Acting Insulin Aspart Improves Glycemic Control in Basal-Bolus Treatment for Type 1 Diabetes: Results of a 26-Week Multicenter, Active-Controlled, Treat-to-Target, Randomized, Parallel-Group Trial (onset 1). Diabetes Care 2017;40:943-950.
8. Mathieu C, Bode BW et al. Efficacy and safety of fast-acting insulin aspart in comparison with insulin aspart in type 1 diabetes (onset 1): A 52-week, randomized, treat-to-target, phase III trial. Diabetes Obes Metab 2018;1-8.
9. Bowering K, Case C et al. Faster Aspart Versus Insulin Aspart as Part of a Basal-Bolus Regimen in Inadequately Controlled Type 2 Diabetes: The onset 2 Trial. Diabetes Care 2017;40:951-957.
10. Rodbard HW, Tripathy D et al. Adding fast-acting insulin aspart to basal insulin significantly improved glycaemic control in patients with type 2 diabetes: A randomized, 18-week, open-label, phase 3 trial (onset 3). Diabetes Obes Metab 2017;19:1389-1396 en_GB/document_library/EPAR_-_Summary_for_the_public/human/004046/WC500220889.pdf
11. Hӧvelmann U, Heise T et al. Pharmacokinetic Properties of Fast-Acting Insuline-aspart administered in Different Subcutaneous Injection Regions. Clin Drug Investig 2017;37:503-509.
12. Bode BW, Johnson JA et al. Improved Postprandial Glycemic Control with Faster-Acting Insulin Aspart in Patients with Type 1 Diabetes Using Continuous Subcutaneous Insulin Infusion. Diabet Tech Therapeutics 2017;19:25-33.
13. Heise T, Zijlstra E et al., Pharmacological properties of faster-acting insulin aspart vs insulin aspart in patients with type 1 diabetes receiving continuous subcutaneous insulin infusion: A randomized, double-blind, crossover trial. Diabetes Obes Metab 2017;19(2):208-215.
14. Zijlstra E, Demissie M et al. Investigating of Pump Compatibility of Fast-Acting Insulin Aspart in subjects with Type I Diabetes. J Diab Science Techn 2018;12(1):145-151.
15. Basu A, Pieber TR et al. Greater early postprandial suppression of endogenous glucose production and higher initial glucose disappearance is achieved with fast-acting insulin aspart compared with insulin aspart. Diabetes Obes Metab 2018;20:1-8.